La intervención que más probabilidad tiene de afectar el resultado final del manejo de cualquier paciente es el lugar donde el paramédico decide transportar al paciente. En este episodio discutimos algunos de los mitos más comunes y cómo corregirlos.
¿Cuál es el problema que usted sospecha en el paciente?
Haga una lista de los posibles diagnósticos diferenciales. Es posible que pueda descartar algunos, pero otros deben quedar pendientes por descartar ("rule out"). Siempre tenga como prioridad el descartar aquellos diagnósticos diferenciales que sean letales si no se diagnostican correctamente.
¿Cómo se trata el problema que usted está sospechando?
Indistintamente de que el paramédico no sea quien realice el tratamiento definitivo, el paramédico tiene que conocer en qué consiste, en términos generales, la disposición final de estos pacientes para así poder entender qué recursos necesita su paciente.
¿Qué hospitales realizan ese tratamiento?
Contrario a lo que muchas personas puedan pensar, las capacidades de los hospitales dependen y varían de una institución a otra. En términos generales, la mayoría cuentan con algunos o todos los servicios generales primarios, tales como una Sala de Emergencias (aunque no todos tienen que tenerlas), servicios de medicina interna, cirugía, pediatría, ginecología, psiquiatría y subespecialidades de estas. Aunque un hospital cuente con un pediatra, si el hospital no cuenta con facilidades de internamiento para pacientes pediátricos, todo paciente que requiera admisión deberá ser transladado a alguna otra facilidad. Ya esto supone un retraso en el acceso al cuidado adecuado.
¿Cuál es el más cercano entre los que realizan ese tratamiento?
En su mente solo existen los hospitale que realizan el tratamiento que su paciente necesita. Usted no transporta a otro lugar que no sea a los que pueden atender a su paciente. Entre los que puedan atender la condición que aqueja a su paciente, usted puede darse el lujo de escoger el más cercano.
Link a Ley EMTALA
Preguntas Clave
Conteste estas preguntas:
Pacientes cardiacos: ¿Cuál(es) es (son) el (los) hospital(es) más cercano(s) que puede(n) realizar intervención coronaria percutánea 24/7 todos los días del año?
Pacientes con sospecha de accidente cerebrovascular (ACV): ¿Cuál(es) es (son) el (los) hospital(es) más cercano(s) queadministra trombolíticos para un ACV o "stroke"?
Pacientes pediátricos: ¿Cuál(es) es (son) el (los) hospital(es) más cercano(s) que cuenta con una Unidad de Cuidados Intensivos Pediátricos?
Pacientes de trauma: ¿Cuál(es) es (son) el (los) hospital(es) más cercano(s) que cuenta con un servicio de cirugía de trauma que cumpla con el estándar de que el cirujano esté en la cabecera del paciente en o antes de los primeros 15 minutos de que el paciente llegó al hospital?
Pacientes de sepsis: ¿Cuál(es) es (son) el (los) hospital(es) más cercano(s) que cuentan con una Unidad de Cuidados Intensivos para Adultos?
Salas de Emergencias Independientes y Facilidades Alternas de Transporte
Son una alternativa cuando no hay nada importante que descartar. No son la facilidad de transporte adecuado cuando el paciente necesita cuidado adecuado inmediato. A pesar de que son operadas por médicos y enfermeros, no cuentan con personal especializado en medicina de emergencias ni cuentan con los recursos necesarios para disponer adecuadamente del paciente. Todo paciente con una condición importante, que acuda a una de estas facilidades, es una transferencia segura a otro hospital... si es que consigue ser transferido.
El manejo de las bradicardias inestables es parte de los temas que discutimos en el curso de Soporte Vital Cardiovascular Avanzado (ACLS). En este episodio discutiremos el algoritmo de manejo del paciente con bradicardias siguiendo las Guías 2015 de la American Heart Association.
En este episodio hablamos sobre el artículo que aparece en la Revista EMS World acerca del uso de torniquetes en incidentes con múltiples víctimas.
Puede ver el artículo completo aquí: http://www.emsworld.com/article/12128614/uso-del-torniquete-en-imvs
Este es el 4to y último episodio del EMS World Expo 2015, grabado en la ciudad de Las Vegas, Nevada. En este episodio comparto con Jamie Davis, el Podmedic, anfitrión del MedicCast y con Chris Montera del EMS Garage.
La fibrilación atrial (conocida por FA, AF, o “afib”) es la arritmia más común. Es probable que usted la vea TODOS los días en una sala de emergencias, la unidad de cuidados intensivos, o un piso de medicina interna. Es importante porque es la arritmia más común, el manejo puede ser complejo. Para entender la fibrilación atrial, es importante entender el problema desde el punto de vista eléctrico y mecánico ya que los pacientes con fibrilación atrial pueden tener episodios de respuesta ventricular rápida y pueden embolizar trombos formados en los atrios.
¿Qué es la fibrilación atrial?
El término consiste en la despolarización masiva de las células del atrio, de forma desorganizada y sin coordinación.
El atrio tiende a fibrilar de forma espontánea cuando se dilata. Los pacientes en fallo cardiaco eventualmente tienen dilatación del atrio, por lo que los pacientes en fallo cardiaco suelen tener fibrilación atrial. Los episodios de fibrilación pueden ser temporeros o persistentes.
Debido a condiciones pre-existentes (tales como fallo cardiaco), algunos pacientes están ya propensos a desarrollar fibrilación atrial. Ante el menor insulto tienden a fibrilar. Por ejemplo, un paciente con sepsis severa puede tener un episodio de fibrilación debido al estrés que tiene el corazón durante el episodio de sepsis. En estos casos, el fallo cardiaco consiste en un problema estructural del corazón y la fibrilación atrial es parte del resultado final.
Respuesta ventricular
El atrio está produciendo cantidades masivas de impulsos eléctricos (posiblemente por encima de los 300 por minuto). El nodo atrioventricular (AV) “filtra” solamente cierta cantidad de impulsos hacia el ventrículo. Cuando el impulso llega al ventrículo el corazón se contrae, y cuando se contrae el corazón bombea sangre hacia afuera. Es por esto que el paciente con fibrilación atrial tiene pulso: el ventrículo se sigue contrayendo y produciendo gasto cardiaco.
La respuesta ventricular dependerá de cuántos impulsos deja pasar el nodo AV. Si el nodo AV permite el paso de muchos impulsos, el ventrículo se contraerá rápido, y viceversa. Aunque la actividad atrial es caóticamente rápida, la respuesta ventricular puede ser lenta, normal o rápida. Debido a que el origen del impulso es caótico, la respuesta ventricular siempre va a ser irregular y sin ningún patrón en su irregularidad (irregularmente irregular).
La respuesta ventricular también va a depender de las necesidades del paciente. Si el cuerpo necesita un gasto cardiaco mayor, va a provocar un aumento natural en la frecuencia cardiaca, lo que puede desatar frecuencias sumamente rápidas debido a la disponibilidad relativamente infinita de impulsos eléctricos en el atrio.
Fisiología normal
Para entender lo que pasa con la fibrilación atrial es necesario entender cómo trabaja el corazón normalmente. La sangre pasa del atrio al ventrículo porque las válvulas se abren. Aunque la mayoría de la sangre pasa al ventrículo, siempre se queda un pequeño remanente (un 20%-30%) en el atrio. Para asegurarse de que ese volumen pasa completamente al ventrículo, el atrio se contrae y entonces el ventrículo se llena completo. El paciente en fibrilación atrial pierde esa contracción atrial. Hay tantas partes del atrio intentando contraerse que la actividad es caótica y el atrio luce como si estuviera temblando.
Cuando el flujo de sangre se detiene, la sangre se coagula. Todos los pacientes con fibrilación atrial tienen el peligro de formar coágulos en el atrio.
Los episodios de fibrilación atrial pueden revertir espontáneamente. Cuando esto ocurre, el atrio vuelve a contraerse normalmente. Cuando el atrio se contrae normalmente, cualquier trombo que se haya formado va a comenzar a embolizar (a viajar por la circulación). Todos los pacientes con fibrilación atrial están en riesgo de tener eventos embólicos tales como accidente cerebrovascular isquémico, trombosis mesentérica, o isquemias en cualquier otra parte del cuerpo.
¿El problema es frecuencia o ritmo?
Como mencionado anteriormente, es común que el paciente que presenta fibrilación atrial tenga, en adición, un historial de fallo cardiaco. Partiendo de la premisa de que el fallo cardiaco es una condición crónica, es razonable asumir que, en muchos pacientes, el (los) episodio(s) de fibrilación atrial llevan ya bastante tiempo. Por ejemplo, una paciente de 70 años de edad, con edema de miembros inferiores, y con ortopnea de 4 almohadas desde varios años es probable asumir que su fibrilación atrial no sea un evento nuevo.
Entonces, ¿por qué decidió venir hoy a atenderse? Una posible razón es simplemente porque “ayer” la paciente tenía una fibrilación atrial con una respuesta ventricular de 80 latidos por minutos, mientras que “hoy” tiene una fibrilación atrial con respuesta ventricular en 180 latidos por minuto. Entonces, la manifestación clínica de la paciente se debe a la frecuencia, no al ritmo. El manejo entonces debe ser dirigido a corregir la frecuencia, y no a corregir el ritmo.
¿Cuál es la causa?
Esa es la verdadera pregunta. Por ejemplo, el desequilibrio electrolítico causado por la deshidratación o hipovolemia puede provocar una respuesta de taquicardia absolutamente normal en todo ser humano. Si encima de esto le sumamos a que el corazón es susceptible a desencadenar episodios de fibrilación atrial, se conjuga la tormenta perfecta. En este caso hipotético, la resucitación adecuada con fluidos y la corrección de los electrolitos se debe encargar del problema, y el episodio de fibrilación atrial debe ser auto-limitado.
En algunos casos, el problema es el corazón, como mencionado anteriormente. Nada está estimulando el episodio de fibrilación atrial. El corazón tiene un problema estructural. Los pacientes con problemas estructurales del corazón tienden a fibrilar fácilmente.
Uno de los retos del manejo del paciente con NOAF (fibrilación atrial de inicio reciente, por sus siglas en inglés) es entender si el episodio de fibrilación atrial es auto-limitado y se irá cuando el insulto que lo está estimulando se resuelva, o esto se debe a un problema estructural que requiere mayor atención.
Diagnóstico
Obviamente el ECG es el método de diagnóstico de la fibrilación atrial. Se pierden las ondas P en el ECG, y a su vez aparecen ondas fibrilatorias donde se supone que estén las ondas P. Las ondas fibrilatorias son caóticas por su naturaleza. La respuesta ventricular es irregular y puede variar.
Pero el verdadero tema del diagnóstico es entender qué está pasando con este paciente en términos generales.
Como mencionado anteriormente, los pacientes con condición cardiaca, tales como enfermedad valvular, infarto al miocardio, fallo de ventrículo izquierdo, pericarditis, y otras cardiomiopatías, pueden desarrollar fibrilación atrial.
Otras causas no-cardiacas que pueden llevar a fibrilación atrial incluyen:
- Embolia pulmonar
- Pacientes post-cirugía torácica
- COPD
- Hipokalemia
- Hipotermia
- Síndrome de seno enfermo
- Tirotoxicosis
- Intoxicación con digitálicos
El consumo de alcohol puede provocar episodios de fibrilación atrial (típicamente llamado Holiday Heart Syndrome).
Clasificación según la duración del episodio
Nos referimos a paroxismos cuando algo ocurre y desaparece espontáneamente. Por lo general una fibrilación atrial paroxística ocurre y termina en cuestión de horas.
La fibrilación atrial persistente dura más de 48 horas y requiere el uso de cardioversión farmacológica o eléctrica para obtener un ritmo sinusal normal.
En algunos casos la fibrilación atrial es permanente y no resuelve con medicamentos o cardioversión.
Cómo tratarla…
Escuche cómo tratarla en el podcast…
Lea sobre el CHADS2 Score http://www.mdcalc.com/chads2-score-for-atrial-fibrillation-stroke-risk/
En este episodio continuamos con las entrevistas realizadas durante la convención anual del EMS World Expo, celebrada en la ciudad de Las Vegas, Nevada. En este episodio entrevistamos al Sr. Héctor "Tito" Fontanez y a Juan Calderón, de la Administración de Servicios Médicos de Puerto Rico.
El manejo de las taquicardias inestables es parte de los temas que discutimos en el curso deSoporte Vital Cardiovascular Avanzado (ACLS). En este episodio discutiremos el algoritmo de manejo del paciente con taquicardias inestables, siguiendo las Guías 2015 de la American Heart Association para el manejo de taquicardias sintomáticas.
En este episodio:
- Jorge Rembis Miranda MHA OMS DDS EMT-P
- Gustavo E. Flores, MD EMT-P
- Ernesto Aguilera Ceciliano EMT-P
- Miguel Ángel Luna
Director EREES
Coordinador regional NAEMT en México
Introducción
El síndrome coronario agudo (SCA) afecta a miles de hombres y mujeres cada día en todo el mundo y es una de las principales causas de muerte súbita. Algunos hospitales cuentan con unidades específicas para el manejo del paciente con dolor de pecho, con el fin de que estas unidades se especialicen en cómo rápidamente diagnosticar y efectivamente tratar el síndrome coronario agudo. La mayoría de los Departamentos de Emergencia de los hospitales no cuentan con una Unidad de Dolor de Pecho. Aunque aun así proveen excelente atención médica, muchos errores se cometen innecesariamente.
El manejo correcto en el momento correcto
Sin embargo, el manejo del paciente con el síndrome coronario agudo comienza desde que llega el personal del Servicio de Emergencias Médicas, cuando el paciente se encuentra fuera del hospital.
Similarmente, algunos pacientes pueden tener las primeras manifestaciones de un SCA estando ya ingresados en el hospital. Desafortunadamente, se ha demostrado que el manejo no es óptimo cuando el paciente muestra los primeros síntomas estando ya ingresado en el hospital. Algunas de las posibles explicaciones es que el personal que trabaja en los diferentes pisos, o pabellones, no tiene la experiencia suficiente en el manejo inicial de estos pacientes. Otra teoría es que la coordinación de los procesos (por ejemplo, la activación del Laboratorio de Cardiología) no está optimizada. El personal a veces tiene que esperar que otro(s) colega(s) de otros departamentos lleguen para poder manejar adecuadamente el paciente.
En cualquier caso. el manejo apropiado tiene que comenzar en el lugar donde se encuentra el paciente.
Error #1: No activar el laboratorio de cateterismo cuando hay sospecha de STEMI o equivalente
Si usted cometiera TODOS los siguientes errores en esta lista, el paciente probablemente va a tener un buen resultado si usted NO comete este primer error.
En algunos casos, el laboratorio de cateterismo está en otro lugar (como es en todos los casos de los paramédicos donde el paciente está fuera del hospital, o el hospital donde se encuentra el paciente no cuenta con capacidad de reperfusión coronaria).
En este error tenemos que incluir el hecho de que en muchos casos los paramédicos NO llevan a los pacientes con síndrome coronario agudo a una sala de emergencias apropiada, es decir, a una sala de emergencias que NO tiene capacidad de reperfusión mediante intervención coronaria percutánea.
El proceso de activar el laboratorio de cateterismo puede varias de un hospital a otro. Algunos ejemplos son:
- El paramédico activa y transmite el ECG a cardiólogo intervencionista
- El médico activa y transmite el ECG al cardiólogo intervencionista
En cualquier caso, el objetivo es que el tiempo desde que el paciente llega hasta que se reperfunda el corazón sea de menos de 90 minutos. Es lo mismo que el paciente espere 30 minutos dentro de la ambulancia de camino al hospital a que el paciente espere 30 minutos en la sala de emergencias en lo que el equipo llega.
Por último, muchos pacientes no van a estar infartando en este preciso momento, pero sí tienen evidencia de oclusión severa y clínicamente significativa. Los pacientes que tienen oclusiones con alta mortalidad se benefician de la reperfusión inmediata. Esto nos lleva al segundo error crítico.
Error #2: No considerar equivalentes e imitadores de STEMI
No todos los pacientes con elevación en el segmento ST en el ECG tienen infarto al miocardio. La discusión de qué pacientes NO tienen infarto al miocardio es más larga y extensa de lo que podemos abarcar en este artículo, por lo que se discutirá en otro artículo más adelante. En un mundo perfecto, los equipos de cardiología, los equipos del Departamento de Emergencia, y los equipos del Servicio de Emergencias Médicas comparten la discusión de casos selectos para el beneficio y aprendizaje de todos. En estas reuniones se discuten los casos para mejorar la capacidad de diagnóstico y manejo apropiado. Esto implica que los cardiólogos deben ser inicialmente pacientes con el proceso de desarrollo de los demás proveedores hasta que se logre alcanzar un porcentaje aceptable de falsos positivos. Los falsos positivos les ocurren a TODOS. No significa incompetencia. En todo caso, ¡significa que se preocupan mucho por sus pacientes!
Abra canales de comunicación y úselos. Si tiene duda sobre un paciente, envíele el ECG al cardiólogo de turno antes de activar la alerta de STEMI. La consulta debe tomar solo algunos minutos pero ayudará a todo el equipo a estar seguros de que están haciendo lo correcto.
Como mencionado anteriormente, por otro lado, muchos pacientes NO tienen elevación de segmento ST, pero sí tienen oclusiones significativas. En este artículo hablamos de los casos donde es necesario activar el laboratorio de cateterismo.
Error #3: No considerar el SCA porque el paciente no tiene los signos típicos
Los signos y síntomas típicos de un SCA incluyen:
- Dolor o molestia en el centro del pecho, con o irradiación al brazo izquierdo
- Dificultad para respirar
- Piel fría, sudorosa y pálida
- Náusea o indigestión
Si usted está esperando a que su próximo paciente con un SCA le muestre todos estos signos, se le van a escapar muchos SCA que no muestran estos signos típicos.
Muchos pacientes pueden no tener estos síntomas, pero en cambio tener otros síntomas que normalmente no son atribuidos a un SCA, tales como dolor de espalda, dolor de abdomen, dolor de cuello, dolor de brazo izquierdo, hipo, debilidad general sin ningún tipo de dolor, etc. ¡Las manifestaciones pueden ser sumamente variadas!
De igual manera, la ausencia de factores de riesgo no descarta que el paciente tenga un síndrome coronario agudo. Muchas personas aparentemente saludables tienen infartos agudos al miocardio sin haber experimentado signos ni síntomas anteriormente.
Error #4: Pensar que solamente MONA es suficiente.
Tradicionalmente se ha recomendado que los pacientes que tienen un SCA reciban Morfina, Oxígeno, Nitroglicerina y Aspirina (MONA), aunque no en ese mismo orden.
Aunque hoy día sabemos que no todos los pacientes requieren oxígeno ni morfina, sí es importante poder administrar nitroglicerina y aspirina siempre que no haya contraindicaciones.
No obstante, estos manejos NO van a producir reperfusión. La aspirina no rompe el trombo. Más bien evita que se agreguen las plaquetas que puedan hacer que se produzca una mayor oclusión. La nitroglicerina dilata las arterias coronarias, pero su mayor beneficio está en reducir la precarga. Estas intervenciones son importantes, pero NO son el objetivo final del tratamiento. Es importante que los pacientes con un infarto agudo al miocardio puedan ser reperfundidos, y esto se puede lograr inicialmente mediante el uso de trombolíticos o una intervención coronaria percutánea.
El hecho de que el paciente ya no tenga dolor de pecho (gracias a la nitroglicerina) no descarta que pueda estar infartando y que necesite intervención coronaria percutánea de inmediato.
Error #5: No realizar EKGs seriados después de que el primero salió normal
Si usted tiene la preocupación de que su paciente puede estar sufriendo un síndrome coronario agudo, tiene que perseguir el diagnóstico mientras va atendiendo al paciente. En muchos casos el EKG inicial (realizado en los primeros 10 minutos de la presentación inicial) muestra cambios indicativos de la oclusión, pero en otros casos el ECG no muestra estos cambios inicialmente.
Los cambios en el ECG ocurren de forma dinámica. Es decir, van cambiando. Según pasa el tiempo, el ECG va mostrando nuevos patrones. La evolución de estos cambios es importante para evaluar la presencia y/o progresión de la enfermedad.
A veces el EKG inicial muestra algunos cambios, que pasan desapercibidos por los proveedores iniciales. No es entonces hasta tiempo después, luego de que la condición va evolucionando, que los nuevos cambios se vuelven más obvios.
En cualquier caso, no se van a ignorar si se vuelve costumbre tomar varios ECGs en pacientes con sospecha de estar sufriendo de un SCA.
Conclusión
Si usted realiza estos 5 errores clásicos, le garantizo que sus pacientes van sufrir. Por otro lado, preocúpese por que usted (ni los integrantes de su equipo) cometan estos cinco errores, y sus pacientes se beneficiarán enormemente.
![9ages[1]](http://www.eccpodcast.com/wp-content/uploads/2015/11/9ages1-150x150.jpg) Uno de los temas más controversiales sobre el manejo de un paro cardiaco es cómo decidir terminar los esfuerzos de resucitación. Como profesionales de la salud tenemos un deseo innato de intentar resucitar a todo paciente en paro cardiaco, pero la vida es eventualmente finita. Una vez aprendí, y nunca he olvidado, que en la medicina tenemos el honor de presenciar dos de los eventos más significativos de un ser humano...su nacimiento y su muerte. Cuando las circunstancias se dan para que estos dos momentos ocurran, van a ocurrir indistintamente de lo que nosotros hagamos para evitarlo. Es nuestro deber honrar este proceso natural. La muerte no siempre representa el fracaso de nuestros esfuerzos, sino el fin de un proceso natural.
Uno de los temas más controversiales sobre el manejo de un paro cardiaco es cómo decidir terminar los esfuerzos de resucitación. Como profesionales de la salud tenemos un deseo innato de intentar resucitar a todo paciente en paro cardiaco, pero la vida es eventualmente finita. Una vez aprendí, y nunca he olvidado, que en la medicina tenemos el honor de presenciar dos de los eventos más significativos de un ser humano...su nacimiento y su muerte. Cuando las circunstancias se dan para que estos dos momentos ocurran, van a ocurrir indistintamente de lo que nosotros hagamos para evitarlo. Es nuestro deber honrar este proceso natural. La muerte no siempre representa el fracaso de nuestros esfuerzos, sino el fin de un proceso natural.
Las Guías 2010 y 2015 de la American Heart Association proveen mucha información sobre los aspectos éticos a considerar a la hora de discutir el tema de detener la resucitación. La intención de este episodio no es discutir los aspectos éticos, aunque hay algunos aspectos que es inevitable considerarlos. No obstante, no es la intención de este artículo discutirlos todos, por lo que los invito a visitar la página de la AHA para las Guías 2015, disponibles gratuitamente en http://eccguidelines.heart.org.
El tiempo no es relevante
El tiempo del intento de resucitación no es el factor principal en la toma de decisiones. Debemos dejar de usar el tiempo para decidir si hemos intentado mucho o poco la resucitación. El uso del tiempo como factor exclusivo denota desconocimiento de los objetivos de la reanimación. ¿Debo mencionarlo nuevamente? El tiempo es un elemento muy subjetivo.
La subjetividad del tiempo
El tiempo es objetivo. Lo medimos con un reloj...segundos, etc... de eso no cabe duda. Podemos medirlo con precisión atómica. Lo que varía es nuestra percepción del tiempo. Aunque parezca irónico, la percepción del tiempo es una de las cosas más subjetivas que hay. Haga usted la prueba... cuando usted quiere que el tiempo corra rápido, toma una eternidad. Viceversa, cuando quiere que el tiempo se detenga, pasa todo muy rápido.
Es común oir frases como "esto acaba de ocurrir ahora mismo"...pero ya van unos 10 minutos. Por otro lado es posible oir "la ambulancia está tardando una eternidad". pero solo han pasado 2 minutos y 35 segundos desde que terminó la llamada al 9-1-1.
¿Cuándo no iniciar la resucitación?
En muchos casos no es apropiado ni siquiera iniciar la resucitación. Tiempo de resucitación = 0 minutos. No se intentó la resucitación.
Algunos ejemplos son:
- Situaciones donde intentar realizar la resucitación pondría al rescatador en peligro
- Directriz avanzada, testamento u orden de no resucitar (DNR)
- Signos obvios de muerte irreversible (decapitación, rigor mortis, descomposición, etc.)
En estos casos, desde el inicio, se sabe que el intento de resucitación va a ser inconsecuente y futil.
Cabe señalar que el no iniciar la resucitación y el dar por terminado los esfuerzos de resucitación son ambos éticamente equivalentes.
Ante la duda, saluda
Ante ausencia de alguna buena razón para no comenzar (ver anterior), siempre que creamos que podemos resucitar al paciente, debemos fallar a favor del paciente e intentar la resucitación.
Pero si fuera así, todavía estaríamos intentando resucitar a los padres de la patria. Tiene que haber una forma para decidir detenerse.
DNR
A veces la mejor forma de detener la resucitación es una forma (formulario) indicando las intenciones del paciente. Nunca es demasiado temprano para comenzar una discusión, en el momento oportuno, con un paciente sobre sus deseos al final de la vida. Es nuestro deber encontrar ese momento oportuno.
Esta página ayuda a las familias a comenzar esta discusión de la manera correcta: http://deathoverdinner.org/
Pero cuando esto no ocurre, el médico debe hacerlo. El programa POLST provee unos fundamentos para lograrlo:
- Conversación entre el paciente, profesionales de la salud, y familiares cercanos
- Toma de decisión compartida entre el paciente y su profesional de la salud acerca de el cuidado que el paciente desea recibir al final de su vida
- Asegurar que los deseos del paciente se cumplan, documentándolo en un formulario
Tenemos que mejorar nuestro conocimiento de cuidado de fin de la vida. Cuidado paliativo no es retirar el cuidado...es proveer comodidad al final de la vida. De igual manera, tenemos que aprender a manejar ese cuidado paliativo una vez se comenzaron a realizar medidas avanzadas, tales como la intubación endotraqueal y ventilación mecánica. El no saber extubar a un paciente en etapa terminal resulta en preguntas erróneas tales como "¿desea que lo intuben"? en vez de "¿desea que lo resuciten?".
El National Institute for Health and Care Excellence del Reino Unido publica sus guías de fin de la vida para adultos, disponibles aquí. En adición, aquí hay un ejemplo de un protocolo de cuidado para la extubación terminal de un paciente: http://www.aacn.org/WD/Palliative/Docs/terminal_weaning_st_thomas.pdf
Como siempre, siga sus protocolos locales.
Los hospitales que miden tazas de sobrevivencia se benefician de tener órdenes de DNR debidamente firmadas ya que estos pacientes terminales entonces no entrarán a los registros de intentos de reanimación.
A veces la evidencia de una orden DNR llega luego que la reanimación ha comenzado. En el caso de los proveedores fuera del hospital, se debe seguir el protocolo local. Si no existe un protocolo de cómo proceder en estos casos, se debe consultar al control médico para detener la resucitación. El objetivo final debe ser respetar los últimos deseos válidos y legítimos del paciente.
Protocolo de Terminación de BLS en paro cardiaco fuera del hospital
En términos generales, la RCP se realiza hasta que:
- Retorno de circulación espontánea
- Transferencia de cuidado a un equipo que provea soporte vital avanzado (en cuyo caso la resucitación puede continuar, pero bajo el control de los nuevos proveedores)
- El rescatador no puede continuar debido a cansancio o riesgo a su seguridad.
- Se cumplen criterios confiables de muerte cerebral irreversible, se identifican criterios de muerte obvia, o criterios para terminar la resucitación.
A nivel de profesionales de BLS, los criterios incluyen:
- El paro cardiaco no fue presenciado por el primer respondedor o proveedor del SEM
- No hay retorno de circulación espontánea luego de 3 rondas de RCP y análisis del DEA
- El DEA no emitió ninguna descarga
Es importante que la decisión se consultada con el médico para detener la reanimación a nivel de BLS. Los proveedores deben ser instruídos acerca de cómo comunicarse con la familia durante este momento de crisis.
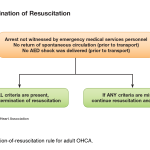
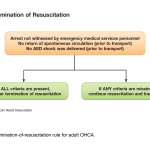
https://eccguidelines.heart.org/wp-content/uploads/2015/10/ACLS-Termination-of-Resuscitation.png
https://eccguidelines.heart.org/wp-content/uploads/2015/10/ACLS-Termination-of-Resuscitation.png
- El paro cardiaco no fue presenciado por el primer respondedor o proveedor del SEM.
- Ningún testigo realizó RCP
- No hubo RCE (retorno de circulación espontánea) luego de un intento completo de resucitación en la escena.
- El AED no recomendó ninguna descarga.
El paciente vive o muere en la escena
La única oportunidad de sobrevivencia del paciente en paro cardiaco es que se obtenga retorno de circulación espontánea en la escena. Las Guías 2015 de la AHA recomiendan que el paciente sea atendido en el lugar donde se encontró.
Es más conveniente, en términos generales, atender al paciente en la misma escena que dentro de la ambulancia ya que en la escena comúnmente hay más espacio y comodidad que en espacio cerrado de la ambulancia.
El paciente que no obtiene retorno de circulación espontánea en la escena tiene 0.7% de sobrevivencia, a diferencia del que sí obtiene RCE, cuya posibilidad de sobrevivencia asciende a un 17.2%. (Prehosp Emerg Care. 2012 Oct-Dec;16(4):451-5)
La RCP durante el transporte es pésima. No produce ningún flujo sanguíneo significativo, pone a los proveedores en riesgo de accidentes, y no está asociado a aumento en sobrevivencia. No se debe realizar RCP en movimiento.
¿Cómo resucitar a un paciente?
Paso 1: Proteger al cerebro mediante compresiones cardiacas
Paso 2: Tratar la causa del paro
¿Por qué su paciente está en paro cardiaco?
Los pacientes en paro cardiaco se pueden dividir, según el algoritmo, en dos tipos: los que tienen un problema de ritmo [arritmias como fibrilación ventricular (FV) y taquicardia ventricular (TV) sin pulso] vs los que no tienen un problema de ritmo. Identificar esto es fácil si se tiene un monitor cardiaco. Una simple revisión rápida del ritmo nos provee esta respuesta.
Todo paciente en paro cardiaco recibe el siguiente tratamiento:
- Compresiones de alta calidad, con la menor cantidad de interrupciones.
- Análisis del ritmo cardiaco inicialmente y cada dos minutos. Si el ritmo es desfibrilable, se desfibrila, si el ritmo no es desfibrilable, no se desfibrila.
- Epinefrina 1 mg cada 4 minutos (3-5 minutos)
- Tratar las causas reversibles probables. (si es una arritmia, se administra un antiarrítmico)
Causas Reversibles
Las causas reversibles son:
- "Heart" (arritmias del corazón) - desfibrilación + antiarrítmicos
- Hivolemia - líquidos y sangre
- Hipoxia - oxígeno
- Hidrógeno (acidosis) - bicarbonato si estaba acidótico antes del paro
- Hipotermia - calentar al paciente
- Hipoglucemia (especialmente en pediátricos) - dextrosa
- Hipo/hiperpotasemia - calcio, bicarbonato, dextrosa + insulina
- Toxinas - antídoto (naloxona si es un opioide, o lo que recomiende el Centro de Envenenamientos 1-800-222-1222)
- Tension, pneumotórax - descompresión
- Tamponada cardiaca - descompresión
- Trombosis coronaria - reperfusión
- Trombosis pulmonar - reperfusión
Volvamos al Paso 1: Proteja al cerebro
Primum non nocere (primero no cause más daño). En este caso, esto significa que no causemos más anoxia al cerebro. Si usted interrumpe las compresiones, pierde perfusión cerebral. Tenemos que volvernos una máquina perfecta de perfusión cerebral... ya sea manual o mecánica.
De la forma en que yo lo veo, tenemos un problema (cualquiera de las H's y T's mencionadas anteriormente), y tenemos una solución. Entre medio del problema y la solución, tenemos un obstáculo: la pobre perfusión al cerebro está acabando con el cerebro rápidamente. En otras palabras, tenemos que actuar rápido. El problema es que algunas de las soluciones requieren TIEMPO. Es fácil y rápido descomprimir un pneumotórax a tensión, pero hacer una embolectomía por una embolia pulmonar, o una intervención coronaria percutánea toma más tiempo del que usualmente tenemos.
Tenemos una solución a esto... RCP mecánico. Existe mucha controversia sobre el rol del RCP mecánico... pero si se decide que el paciente requiere un cuidado definitivo que va a durar más tiempo, no hay duda que las máquinas que proveen compresiones continuas tienen esa ventaja: proveer compresiones por largo tiempo.
Lea este artículo de EMSWorld: qué hacer cuando su paciente en RCP mecánico recupera conciencia durante las compresiones. Sin leer el artículo, deducimos que la perfusión al cerebro fue tan buena que el paciente recuperó conocimiento durante las compresiones.
Pero lo más importante de esto, en mi opinión, es que si podemos mantener el cerebro con buena perfusión infinitamente, tenemos un tiempo infinito para tratar de corregir la causa que tiene el paciente.
Antes no nos enfocábamos mucho en la calidad de las compresiones. Las compresiones eran malas (y siguen siendo malas en muchos sitios) y esto provocaba que no hubiera buena perfusión cerebral. A su vez, esto provocaba daño cerebral en poco tiempo. Por lo tanto, antes, el tiempo era importante porque estaba asociado a muerte cerebral. Debido a las pobres compresiones, en pocos minutos empezaba a ocurrir acidosis respiratoria y era necesario tratar la acidosis. Ahora, la acidosis respiratoria se corrige gracias a las buenas compresiones. Ahora, si podemos perfundir perfectamente al paciente, hemos quitado la barrera. El tiempo no es el problema.
El verdadero problema ahora es entender si hay algo que podamos hacer por el paciente. Si existe la posibilidad de hacer algo, se intenta. Si no existe la posibilidad, entonces es momento de suspender el esfuerzo. No es un asunto de tiempo, es un asunto de entender qué tiene el paciente y cuáles son las opciones reales.
Es decir, el tiempo era el factor limitante. Si podemos perfundir perfectamente al paciente, hemos quitado la barrera.
Escuchen este podcast sobre la embolia pulmonar que sufrió el Dr. Joseph Ornato, MD FACEP FACC FAHA. El Dr. Ornato es uno de los principales investigadores sobre el uso de oxigenación por membrana extracorporea (ECMO) durante paro cardiaco para realizar embolectomías. ¡Resulta que él fue uno de sus propios pacientes en su propio estudio! Óigalo contar su historia, la cual incluyó ECMO, compresiones cardiacas, hipotermia terapéutica por 1 semana, y una recuperación neurológica completa.
Las guías 2015 de la AHA recomiendan que la RCP extracorpórea (ECPR) puede proveer tiempo adicional para tratar causas reversibles del paro cardiaco (tales como síndrome coronario agudo, embolia pulmonar, fibrilación ventricular refractaria, hipotermia extrema, intoxicación por drogas, y otras causas más). Lea más sobre ECPR en este website: http://edecmo.org/
El tiempo no es el factor determinante de cuándo detenemos la resucitación. Se detiene el esfuerzo cuando se han intentado las cosas que razonablemente se pueden intentar y no ha habido una respuesta. Se detiene la RCP cuando no hay más nada que hacer.
Paro cardiaco por trauma
Analicemos un caso hipotético:
Los paramédicos llegan 8 minutos luego de que se reporta un serio accidente. Cuando llegan, el paciente está inconsciente, sin signos de vida. ¿Qué posiblemente le pudo haber pasado a este paciente?
Probablemente una o varias de las siguientes:
- Lesión traumática cerebral
- Hipovolemia por un sangrado masivo
- Hipoxia
- Pneumotórax a tensión
- Tamponada cardiaca
¿Cuánta RCP y epinefrina va a resolver estos problemas anteriores? NINGUNA!
Si su paciente se desangró, le administraron líquidos IV, sangre, no ha respondido y está en asístole, ¿cuál es el objetivo de realizar RCP por 20, 30, 60 minutos? De seguro usted realizó estas intervenciones mucho antes de 20 minutos. Si usted ya ha determinado que no hay respuesta y está en asístole... ¿cuánta RCP es necesaria? Probablemente ninguna. Si alguien necesita darle RCP por 30 minutos... pues que lo haga hasta que se sienta que "hizo todo lo posible".
En un futuro, los libros de historia de la medicina mirarán esta época y contarán que:
En el siglo 21 tuvimos una especie de "ritual de paso" para declarar a una persona muerta y dejarla descansar en paz. En este "ritual" le brindámanos epinefrina y ceremonialmente contábamos mientras comprimíamos el pecho rítmicamente y danzábamos alrededor del paciente realizando diferentes procedimientos como desfibrilación, intubación, canalización, etc., hasta que por fin decidíamos, por diferentes y siempre cambiantes razones, que debíamos parar.
En cambio, si usted decide hacer algo, ¡realice intervenciones significativas!
¿Qué son intervenciones significativas?
Las "intervenciones significativas", según John Hinds, son aquellas que directamente arreglan algo. Son intervenciones o acciones específicas. En momentos de crisis, donde el tiempo y los recursos pueden ser limitados, es críticamente importante que todas las personas envueltas no pierdan tiempo en cosas que no sean intervenciones significativas.
Según el Dr. Hinds, las intevenciones significativas en el paciente de trauma son:
- Intubación usando un "bougie" y capnografía de onda
- Toracostomía digital (con el dedo) bilateral
- Colocar una faja pélvica (SAM Splint)
- Enderezar fracturas de huesos largos
- Administrar bolos de fluído (administrar sangre si está en el hospital)
Luego de realizar esto, entonces analizan cuál es el estatus del paciente y cuáles son los problemas que se han descubierto para decidir cuáles son las alternativas (ver abajo más info sobre toracotomía de emergencia y sobre REBOA).
(Nota: El Dr. Hinds falleció en un accidente de motora este año. Vea un tributo aquí).
Pero dejemos que sean las propias palabras del fenecido John Hinds que describan lo que él mismo llamó "intervenciones significativas".
Paro cardiaco por trauma... toracotomía de emergencia
Si usted entiende que su paciente tiene un sangrado masivo, la mejor forma de estabilización es detener el flujo pinzando la aorta. Si usted está decidiendo resucitar al paciente de trauma y se va en paro cardiaco frente a usted... este es el momento. De lo contrario, recuerde que las compresiones cardiacas y la(s) epinefrina(s) son completamente inútiles en este momento.
La toracotomía de emergencia está asociada a mortalidad excesivamente altas. El problema no es solamente encontrar la aorta, sino resolver lo que uno encuentre. Si usted no va a hacer esto, y su paciente requiere un control inmediato de un sangrado masivo abdominal, entonces considere si es útil continuar los esfuerzos.
REBOA: una opción en el futuro cercano
Donación de órganos
En lugares que tengan un sistema de captación inmediata de órganos y un programa preparado para implementarlo efectivamente, los pacientes que no logran RCE podrían ser candidatos para donar hígado y riñones.
Corazones muy buenos para morir
A todos nos corre la adrenalina por las venas cuando llegamos a un paro cardiaco. La mejor satisfacción es ver a un equipo verdaderamente coordinado realizando un esfuerzo genuino e inteligente por corregir la causa. Aunque el obtener el pulso (retorno de circulación espontánea, o RCE) NO es el objetivo final (el objetivo final es lograr el egreso del hospital neurológicamente intacto o viable), el RCE es un paso importante en el progreso del paciente.
A los que nos apasiona ese juego entre la vida y la muerte, saben que una de las mejores emociones es saber que puedes revertir el paro cardiaco, intentarlo, y luego de esforzarte, obtener ese retorno de circulación, sentir el pulso y ver una presión sanguínea en el monitor. A los que me conocen y han trabajado conmigo, saben que usualmente mi frase favorita es "¡buen trabajo mi gente... estamos en cancha todavía!"
Conclusión...memento mori
Recuerde que todos vamos a morir algún día, y si hacemos las cosas correctamente, la muerte puede ser tan digna como la vida.
Referencias
American Heart Association. Web-based Integrated Guidelines for Cardiopulmonary Resuscitation and Emergency Cardiovascular Care – Part 3: Ethical Issues. ECCguidelines.heart.org.
Introducción
El manejo avanzado de la vía aérea es una de las destrezas que definen a todo profesional que trabaje en un entorno de emergencias y cuidado crítico. Aunque existen diversas maneras de lograr una ventilación efectiva, la intubación endotraqueal está asociada a mayor mortalidad si se realiza por operadores sin el conocimiento y experiencia necesaria, indistintamente de dónde sea que trabajen. El manejo de la vía aérea conlleva riesgos. Vea este episodio anterior sobre cómo evaluar los peligros de la vía aérea. El debate eterno ha sido si los paramédicos deben poder intubar, o si es mejor retirar el tubo endotraqueal de las ambulancias. Mi respuesta es... depende.
Intubación asistida farmacológicamente
No es común que una persona alerta y consciente tolere una laringoscopía sin ningún tipo de asistencia farmacológica. El uso de medicamentos para sedar y paralizar a un paciente para lograr las mayores tazas de éxito es una de las herramientas más comúnmente utilizadas. Vea este episodio donde se discute cómo realizar la intubación en secuencia rápida.
Sin embargo, el uso de estos medicamentos trae los riesgos mencionados anteriormente en los otros episodios. Por esta razón, muchos sistemas de respuesta a emergencias no cuentan con estos medicamentos disponibles. Esto crea un círculo vicioso... se decide intubar al paciente, pero como no hay los medicamentos necesarios, la intubación se hace sin asistencia adecuada. Esto complica el proceso y aumenta la posibilidad de que el paciente no pueda ser intubado. Lógicamente, las estadísticas de fracaso en el manejo de la vía aérea son mayores en este entorno.
Todo o nada
Por esta razón, los sistemas que decidan realizar intubación endotraqueal en un paciente consciente deben poder realizar intubación en secuencia rápida con todos los medicamentos necesarios para realizarlo correctamente.
Hay riesgos inherentes al uso de estos medicamentos. Si el director médico del sistema entiende que el sistema no está preparado para mitigarlos, entonces el director médico no debe autorizar su uso, y por ende la intubación endotraqueal no debe formar parte de las alternativas por ese proveedor.
En otras palabras, los paramédicos sí deben poder intubar, pero para hacerlo, es necesario que tengan todos los medicamentos que permitan versatilidad ante diferentes entornos, y la capacidad demostrada para usarlos correctamente. De lo contrario, los tubos endotraqueales no deben estar en las ambulancias.
El detalle están en las letras pequeñas
El permitir que los paramédicos puedan utilizar medicamentos requiere un programa de formación, credencialización, mantenimiento de competencias, y control de calidad en
El permitir que los paramédicos puedan intubar no es solamente escribir un protocolo, comprar los equipos y medicamentos. Requiere educación y evaluación de lo que ocurre en incidentes reales. La mayoría de los programas de formación en manejo de vía aérea consisten en aprender a hacer la laringoscopía y colocar el tubo.
Equipos de monitoreo y obtención de datos
Los equipos de monitoreo multiparámetros permiten evaluar continuamente a los pacientes. Este es el estándar de cuidado porque permite conocer en todo momento cuál es la situación fisiológica del paciente para que el operador tome las decisiones correctas. Por otro lado, permite obtener data de lo que ocurre en la "vida real" para que los administradores del programa de control de calidad puedan utilizar esta data para realizar una retroalimentación más individualizada, medible y efectiva.
Conclusión
Todo el que deba poder realizar una intubación endotraqueal tiene que tener a su disposición todos los equipos y medicamentos necesarios para poderlo realizar. El sistema que permita esto tiene que hacerlo luego de haber validado y credencializado al personal en los conocimientos y destrezas asociados a la intubación endotraqueal asistida con medicamentos.
De lo contrario, no se debería permitir que se realice la intubación endotraqueal...todo o nada.
¿Qué es RSI?
La intubación en secuencia rápida (RSI, por sus siglas en inglés), consiste en la administración casi simultánea de un agente de inducción y un bloqueador neuromuscular con la intención de producir una inconsciencia rápida y flácida para facilitar la intubación endotraqueal de emergencia.
Criterios de manejo de la vía aérea
En términos generales, existen tres criterios generales para decidir manejar la vía aérea de emergencia:
- Fallo en mantener o proteger la vía aérea
- Fallo en la respiración y oxigenación
- Futuro clínico anticipado
¡Cuidado con la presión positiva!
El aire se mueve dentro y fuera del cuerpo realmente por motivos muy simples. El diafragma desciende, y los músculos intercostales elevan las costillas, creando una presión negativa dentro del tórax. El vacío que se crea atrae aire tan pronto la glotis se abre. Entonces el diafragma se relaja y sube, e igual manera se relajan los músculos intercostales, provocando presión positiva dentro del tórax que expulsa el aire dentro de los pulmones hacia afuera.
El movimiento de aire dentro y fuera de los pulmones ocurre por principios básicos de física. El aire se mueve de donde hay alta presión a baja presión. El aire entra a los pulmones por presión negativa. La presión negativa ocurre principalmente dentro del pulmón por lo que el aire no tiene que irse rutinariamente hacia el estómago.
Sin embargo, cuando ventilamos a alguien con un dispositivo bolsa-mascarilla, lo hacemos con presión positiva. Ese aire a presión buscará irse por todas las opciones posibles: tráquea y esófago. El aire que se va a esófago provoca distención gástrica. La distención gástrica provoca que el paciente vomite, lo que aumenta las posibilidades de que el paciente broncoaspire. Es irrelevante el contenido gástrico si el paciente no ha comido nada (NPO) por las últimas 6 horas. Este es el caso de una intubación que se realiza en el quirófano con el objetivo de poder hacer un procedimiento quirúrgico. Sin embargo, la razón invariable por la cual se intuba a alguien fuera del quirófano es porque el paciente no puede respirar, y esto significa que el paciente podría tener un estómago lleno.
Por lo tanto, es sumamente importante ventilar con un volumen y una frecuencia adecuada para evitar la distención gástrica cuando el aire se irá tanto por la tráquea como por el esófago.
El principio de la intubación en secuencia rápida es NO tener que realizar ventilación con presión positiva luego de que el paciente quede inconsciente por el agente de inducción. Si se evita tener que realizar ventilación con presión positiva, disminuye el riesgo de aspiración. Para poder dormir al paciente y realizar la intubación sin necesidad de ventilar al paciente entre medio es necesario crear unas reservas de oxígeno mediante la preoxigenación.
La preoxigenación es necesaria
El cuerpo humano está diseñado para respirar oxígeno al 21% y nitrógeno en un 79% (y cierta fracción de otros gases inertes). Pero cuando comenzamos a respirar concentraciones de oxígeno por encima del 21%, el cuerpo comienza a saturar los tejidos del cuerpo con ese oxígeno. Esto provoca una reserva que será poco a poco liberada cuando el paciente deje de respirar.
Esto quiere decir que aún cuando el paciente no esté respirando, los tejidos del cuerpo irán liberando poco a poco esas reservas de oxígeno. La saturación periférica de oxígeno (SpO2) se mantendrá lo suficientemente alta (por encima de un 90%) en la mayoría de los pacientes por un tiempo significativamente prolongado si el paciente ha recibido al menos 2-5 minutos mínimos de pre-oxigenación. Esto es una pieza clave en el proceso de inducción e intubación ya que reduce la ansiedad de tener que colocar el tubo rápido. En realidad la preoxigenación nos compra tiempo que puede ser medido inclusive en minutos.
Por lo tanto la preoxinenación disminuye el riesgo de aspiración ya que permite poder dormir al paciente y posicionar el tubo sin necesidad de tener que ventilarlo con presión positiva entre medio... teóricamente.
La preoxigenación funciona en la mayoría de los pacientes. Sin embargo siempre hay circunstancias donde el uso de una mascarilla simple no es suficiente. Algunas técnicas recientes contemplan el uso de CPAP para optimizar la capacidad de oxigenación en pacientes que tienen un fallo respiratorio marcado. En este caso el uso del CPAP está diseñado para mejorar la habilidad de llegar hasta el alveolo para poder oxigenar adecuadamente la sangre.
Esto requiere que haya un flujo sanguíneo adecuado. La preoxigenación no va a funcionar si no hay un flujo adecuado. Si hay un desvío de la sangre, o una obstrucción en la perfusión hacia el pulmón, entonces la preoxigenación no va a ser efectiva. Igualmente, tiene que haber una capacidad adecuada de transporte de oxígeno en la hemoglobina.
Es entendible que muchos de los pacientes que necesitan ser intubados de emergencia no tienen una fisiología normal. Es por esto que la intubación nunca es la primera alternativa. Es necesario optimizar primero la perfusión del paciente y la capacidad de respirar lo más que se pueda antes de optar por realizar una intubación.
Adaptación mutua
La intubación endotraqueal no es un proceso benigno y sin complicaciones. Si el paciente está hipóxico, el realizar la intubación endotraqueal puede retrasar el momento en que comienza a ser ventilado y a recibir el oxígeno que necesita. Simultáneamente, otras complicaciones comienzan a ocurrir tales como desaturación, bradicardia y paro cardiorespiratorio.
Para evitar esto hay que llegar al punto medio ideal en donde se encuentra el resultado del esfuerzo por optimizar la respiración del paciente y donde se encuentra el esfuerzo por mitigar los efectos adversos de la intubación.
Nadie fallece porque no lo intuban. Fallece porque no lo ventilan. Por ende, es importante que se comience con optimizar la respiración del paciente según mencionado anteriormente. Si la perfusión y la preoxigenación están bien, el paciente podría aguantar mejor el procedimiento. Si hipotéticamente hablando el dedo gordo del pie es el lugar más remoto y difícil de perfundir, un dedo gordo del pie que se encuentre rosadito y calientito sugiere un mejor estado hemodinámico que un paciente frío y cianótico. Hay que optimizar la hemodinámica del paciente lo más que sea posible antes de intentar someter al paciente a la estimulación vasovagal de la laringoscopía y la falta de ventilación por un determinado tiempo.
Por otro lado, el paciente tendrá alguna situación particular dentro de su condición que podría hacer la intubación más compleja. Por ejemplo, los pacientes con aumento en la presión intracraneal no deberían tener aumentos súbitos en dicha presión durante la laringoscopía. Similarmente, los pacientes hipovolémicos no deben recibir medicamentos que puedan disminuir aún más su presión.
Nos queremos adaptar a las necesidades del paciente y queremos que el paciente esté en las mejores condiciones para ser intubado.
Ventajas de la Inducción Rápida
El RSI permite un control rápido de la vía aérea. Como discutiremos en breve, la administración virtualmente simultánea de los medicamtos de inducción tienen como propósito reducir lo más posible el tiempo que el paciente permanece en apnea antes de poder ser ventilado mediante el tubo endotraqueal.
El RSI minimiza el riesgo de aspiración.
En este episodio discutimos una forma de realizar la intubación en secuencia rápida. Existen otros abordajes como el DSI (delayed sequence intubation, usando CPAP, y otras estrategias, pero en este episodio comenzamos con RSI).
Introducción
Hoy día uno de los mejores métodos para realizar la intubación endotraqueal de emergencia en un paciente consciente y respirando es la intubación en secuencia rápida. Sin embargo, este procedimiento puede tener complicaciones. Es importante poder anticiparlas y evitarlas.
En pacientes sin ningún tipo de complicaciones, el proceso de asegurar la vía aérea puede ser peligroso por un número de motivos:
- El reflejo nauseoso impide que se pueda realizar una laringoscopía.
- El reflejo nauseoso y/o la combatividad de un paciente puede producir un aumento en la presión intracraneal.
- La laringoscopía puede estimular un tono vagal excesivo, provocando bradicardia, hipotensión o paro cardiorespiratorio.
- El proceso de laringoscopía puede retrasar significativamente la ventilación del paciente, resultando en un aumento en la hipoxemia.
- La pobre visualización de las cuerdas vocales durante la laringoscopía puede aumentar las posibilidades de una intubación esofágica, que a su vez está asociada a complicaciones fatales si no se reconoce a tiempo.
- En adición, intentos repetitivos de laringoscopías fallidas pueden resultar en traumas a la orofaringe y estructuras sensibles tales como epiglotis (edema) y tráquea (laceración).
Hay que sopesar los riesgos y beneficios de optar por manejar la vía aérea por intubación endotraqueal.
Nadie fallece porque no lo intuban. Fallecen porque no lo ventilan.
En un capítulo exclusivamente sobre técnicas de manejo de vía aérea, el mejor método para asegurar la vía aérea sería la intubación endotraqueal. Pero esto no significa que el mejor método para asegurar la ventilación en determinadas circunstancias sea la intubación endotraqueal. El objetivo no debe ser colocar un dispositivo en específico, sino garantizar una ventilación efectiva. Nadie fallece porque no lo intuban. Fallecen porque no lo ventilan.
Ventilación manual es una destreza básica
El método de ventilación inicial de excelencia es el resucitador manual (dispositivo bolsa-mascarilla). Es posible ventilar a la mayoría de los seres humanos, en circunstancias normales, con un dispositivo bolsa-mascarilla por un tiempo significativamente prolongado. En ocasiones es imposible ventilar efectivamente con un dispositivo bolsa-mascarilla y se hace necesario realizar un procedimiento más avanzado.
Es fundamental que todo profesional de la salud que trabaje en un entorno de emergencias y/o cuidado crítico pueda realizar una ventilación manual de forma efectiva. De lo contrario, estará sometiendo al paciente a la "necesidad" de realizar un procedimiento más avanzado...y que tiene más riesgos. La ventilación con bolsa mascarilla es una destreza básica. Solo porque es una destreza básica no significa que nuestro nivel de destreza debe ser básico.
Plan A ---> Plan B ---> ¿Plan A?
Si su plan A fue ventilar con bolsa mascarilla pero fue inefectivo, entonces tendrá que pasar al plan B, que bien podría ser tener que intubar al paciente. Si la intubación fracasa, la mayoría de los operadores tienen solo una alternativa: regresar a la ventilación con bolsa mascarilla, ¡que fue el método que les falló poco antes de intentar intubar!
Si usted quiere realizar procedimientos avanzados de la vía aérea, es críticamente importante que usted domine a la perfección el arte y ciencia de ventilar con un dispositivo bolsa-mascarilla. Recuerde que esto es lo que le va a salvar la vida a su paciente...¡y a usted!
Criterios para asegurar la vía aérea
En su forma más elemental, podríamos decir que existen tres criterios para asegurar la vía aérea de un paciente:
- Fallo en mantener o proteger la vía aérea
- Fallo en ventilación y oxigenación
- Futuro clínico anticipado
¿Podría ser difícil?
Luego de analizar los riesgos y beneficios de realizar la intubación, cuando se toma la decisión de intubar es necesario considerar si hay algún factor que pueda hacerla notablemente más difícil en su paciente en particular.
¿Podría ser difícil...
- ventilar con resucitador manual (dispositivo bolsa-mascarilla)?
- realizar la laringoscopía?
- realizar una cricotirotomía?
Existen diferentes formas de estimar si la vía aérea puede ser difícil. Vea algunos ejemplos aquí.
Su vía aérea podría ser un LIMON.
- Luce difícil
- Identificar 3-3-2
- Mallampati >3
- Obstrucción / Obesidad
- No puede mover el cuello
Luce difícil
Si luce difícil, posiblemente lo es.
Algunos factores que hacen que la vía aérea sea difícil incluyen:
- trauma maxilofacial
- mandíbula corta
- lengua grande
- cuello corto
- dientes grandes
Identificar 3-3-2
Trate de colocar:
- 3 dedos entre los dientes del paciente
- 2 dedos en distancia tiromental
- 2 dedos entre el hioide y tiroide
Si puede colocar los dedos, hay un espacio suficientemente grande para desplazar la lengua.
Mallampati
Esta prueba no está validada en un paciente acostado y poco cooperador, por lo tanto su utilidad es muy limitada excepto en los pacientes donde la intubación es programada de emergencia.
Una escala de Mallampati de 3 o más sugiere que habrá poca visibilidad de las estructuras.
Obstrucción / Obesidad
La obstrucción en la vía aérea puede hacer que la colocación del tubo sea difícil o imposible. Algunos signos de obstrucción en la vía aérea pueden ser:
- Alteración súbita y reciente en la voz
- Dificultad en pasar secreciones
- Estridor
Uno de los principales factores para lograr el éxito en la intubación endotraqueal en el primer intento es poder visualizar la laringe (propiamente llamado laringoscopía). La obesidad puede hacer que los ejes visuales no estén alineados. Si los ejes no están alineados es físicamente imposible poder realizar la laringoscopía sin una cámara de video.
No puede mover el cuello
La hiperextensión del cuello permite alinear adecuadamente y más fácilmente los ejes. Algunos pacientes no pueden mover el cuello debido a problemas crónicos o trauma a las vértebras cervicales.
Es posible realizar la laringoscopía sin mover el cuello...pero esto requiere más práctica. Todo operador de la vía aérea debe practicar la laringoscopía en situaciones de poco movimiento del cuello, y practicarlo hasta el punto de que se sienta cómodo(a) al realizar este procedimiento bajo estas condiciones.
Si sospecho que es difícil, ¿qué hago?
Una intubación difícil no es razón para no considerar intubar al paciente. El verdadero problema es no poder ventilar al paciente si la intubación es fallida.
Si hay la posibilidad de que la ventilación con bolsa-mascarilla sea difícil, que la laringoscopía sea difícil y/o que realizar una vía aérea quirúrgica sea difícil, entonces uno debe contemplar si podrá ser posible ventilar al paciente en el caso de que la intubación sea fallida.
Evite buscar problemas si puede evitarlos. Si usted cree que podría no poder ventilar al paciente, puede considear alternativas como una intubación despierta u otros métodos de rescate.
Referencias
https://www.resus.com.au/blog/the-lemon-approach-for-predicting-the-difficult-airway/
http://www.ncems.org/pdf/AppI-DifficultAirwayEvaluation.pdf
http://www.acep.org/content.aspx?id=33992
http://medind.nic.in/iad/t05/i4/iadt05i4p257.pdf
http://www.medscape.com/viewarticle/430201_2
http://lifeinthefastlane.com/ccc/difficult-airway-algorithms/
El International Liaison Committee on Resuscitation (ILCOR) revisa la literatura científica sobre resucitación cardiopulmonar y publica un resumen del consenso sobre la ciencia. Cuando el consenso en base a la ciencia permite hacer alguna recomendación, ILCOR emite recomendaciones basadas en la evidencia para que los diferentes concilios alrededor del mundo las utilicen para formular sus propias guías locales. Las Guías de la American Heart Association (AHA) son las guías más conocidas y utilizadas a nivel mundial.
En el 2010, la American Heart Association realizó la revisión más grande hasta la fecha de la literatura científica. Gracias a ese esfuerzo, las Guías 2015 se concentraron solamente en las áreas importantes donde ha habido evidencia significativa. Las recomendaciones actuales son una combinación de las Guías 2010 y las Guías 2015. Para facilitar la lectura de ambas recomendaciones simultáneamente, AHA publicó un portal de las Guías 2015 en donde aparece la combinación de ambas guías simultáneamente para integrar las recomendaciones en el contexto adecuado.
En esta edición de las Guías 2015, la AHA utilizó la metodología GRADE para evaluar la evidencia y emitir recomendaciones. En vista de esta nueva metodología, la clasificación de la evidencia y los niveles de recomendación cambiaron a pesar de que el texto de la recomendación sigue igual. Por lo tanto, algunos cambios en las recomendaciones consisten en nueva clasificación de la data, y no una acción diferente. La clasificación de la evidencia y la clasificación de las recomendaciones se hace en vista de la evidencia hasta la fecha. Lo que en un pasado pudo haber sido "evidencia contundente" quizás podría ser "cuestionable" en vista de nuevos estudios, y por ende la fuerza de la recomendación debe cambiar correspondientemente.
En este artículo exploramos solamente los cambios al soporte vital básico (BLS, por sus siglas en inglés). Note que la fuente oficial de las guías es eccguidelines.heart.org. Este artículo sirve solamente como discusión adyuvante.
En este artículo exploramos solamente los cambios al soporte vital cardiovascular avanzado (ACLS, por sus siglas en inglés). Note que la fuente oficial de las guías es eccguidelines.heart.org. Este artículo sirve solamente como discusión adyuvante.
Monitoreo del Paciente
La identificación temprana del paciente que está en riesgo de muerte es un elemento fundamental para prevenir el paro cardiaco intrahospitalario. Es por esto que la AHA ha publicado una versión nueva de la cadena de sobrevivencia, esta vez para el paro cardiaco intrahospitalario.
El monitoreo efectivo del paciente en riesgo de muerte, y la notificación temprana al equipo de respuesta rápida (o de paro cardiaco) es fundamental. Una vez en paro cardiorespiratorio, el equipo debe continuar con las medidas básicas y avanzadas para restablecer circulación y continuar al eslabón de cuidado avanzado pos-paro.
El monitoreo del paciente durante el paro cardiaco es otro componente crítico. El monitoreo de parámetros permite validar la calidad de las intervenciones importantes. Por ejemplo, el uso de capnografía, presión arterial, y la saturación central de oxígeno pueden servir para guiar la terapia con vasopresores y detectar el retorno de circulación espontánea.
American Heart Association. Web-based Integrated Guidelines for Cardiopulmonary Resuscitation and Emergency Cardiovascular Care – Part 7: Adult Advanced Cardiovascular Life Support. ECCguidelines.heart.org
Otro ejemplo importante de uso efectivo de tecnología es el ultrasonido (también conocido como sonografía o ecocardiografía). El sonograma en tiempo real permite evaluar objetivamente la presencia de hipovolemia clínicamente significativa, pneumotórax, tromboembolismo pulmonar y tamponada cardiaca.
Inicio de la resucitación
El rescatador solitario no debe interrumpir las compresiones mientras llegan los demás integrantes del equipo de resucitación...
Escenario
Un paciente de 52 años se quejó de dolor de pecho, náuseas y dificultad para respirar. El ECG de 12 derivaciones mostraba un infarto extenso al miocardio con elevación del segmento ST (STEMI) de la pared anterior. Mientras era evaluado, pierde el conocimiento. El monitor cardiaco muestra fibrilación ventricular. Luego de varios minutos de RCP y desfibrilación cada 2 minutos, el paciente tiene pulso palpable, aunque todavía no respira espontáneamente, por lo que las respiraciones continuan manualmente a una frecuencia de 10 por minuto manteniendo así una saturación periférica de oxígeno de 97%. La presión arterial es 73/28 inicialmente. El paciente recibe 1 litro de volumen y es comenzado en infusión de un vasopresor para subir la presión. Debido a que el paciente no responde a comandos verbales, se decide iniciar hipotermia terapéutica manteniendo la temperatura en 36 grados C. El paciente fue intubado, puesto en ventilación mecánica y transferido al laboratorio de cateterismo para reperfundirlo mediante una angioplastía de emergencia.
Lo que acaba de leer parece indicar que el paciente "sobrevivió", pero realmente no sabemos todavía cuál es el estatus neurológico de este paciente. Cuando hablamos de sobrevivencia, nos referimos a que el paciente haya sido egresado del hospital con un nivel funcional adecuado.
Una de las razones por la cual el paciente va a poder sobrevivir va a ser porque se evita que el cerebro tenga un segundo insulto luego de haber sufrido una isquemia y/o anoxia global.
Hipotermia, ¿tenemos que hacerla?
El Síndrome Pos-Paro Cardiaco es una entidad parecida a la sepsis donde se puede ver una respuesta inflamatoria que, entre otras cosas, puede causar fiebre en el paciente pos-paro. Las guías 2010 reconocieron esto y recomendaron que el paciente sea inducido a hipotermia terapéutica entre 32 y 34 grados Centígrados por al menos 12-24 horas.
33 vs. 36 grados C
Un importante estudio reciente comparó la temperatura meta de 33 grados vs. 36 grados y no encontró diferencia significativa. Es decir, ambos ayudaron al paciente pos-paro que no responde a comandos verbales.
Las Guías 2015 de la American Heart Association flexibilizan la recomendación de hipotermia terapéutica. Antes la recomendación era mantener al paciente entre 32-34 grados C. Ahora la recomendación es entre 32-36 grados C.
¿Qué pensaría usted si el 0% de sus pacientes en paro cardiaco sobreviven?
Posiblemente esta sea la realidad de muchos lugares. ¿Cuál es la estadística de sobrevivencia para muerte súbita en su jurisdicción o facilidad? Si usted no la sabe, ¡para todos los efectos es cero (0%), porque no la sabe! Un estimado a base de su intuición o experiencia no es una alternativa aceptable.
Secreto a voces
Quizás un pobre resultado en las estadísticas de sobrevivencia eran de esperarse... y quizás eso desmotiva al equipo a medirlas ya que anticipan que no van a ser resultados positivos.
Cuando un resultado es positivo, lo muestran a todos con orgullo. Pero cuando un resultado es negativo, lo ocultan usualmente. Sin embargo, ese resultado negativo abre la puerta a una oportunidad que antes no se percibía: realizar ajustes para lograr mejorar el resultado. El haber obtenido el resultado negativo quizás es el mejor resultado que pudieron haber tenido porque presenta el problema. Ya no es un secreto a voces. Ahora se puede decidir realizar cambios en las diferentes variables que afectan el resultado y volverlo a medir hasta que lo mejoran. Si no miden, no pueden mejorarlo... no hay forma de saber que estás mejorando si no estás midiendo.
Los vasopresores e inotrópicos son medicamentos sumamente útiles en circunstancias apropiadas. Para entender el efecto de medicamentos vasoactivos es necesario conocer cuáles receptores se encuentran en los vasos sanguíneos y en el corazón.
Receptores alfa
- Aumentan tono arterial (aumentan el MAP)
- Aumentan tono venoso (aumentan la precarga)
Receptores beta
- Aumentan frecuencia cardiaca (cronotrópicos)
- Aumentan contractilidad cardiaca (inotrópicos)
- Vasodilatación arterial
- Broncodilatación
Receptores dopaminérgicos
- Estimulan diuresis
- Aumentan frecuencia cardiaca
- Aumentan contractilidad cardiaca
Entender cómo usar los vasopresores puede ser un tema confuso al principio. En una serie de episodios trataré de presentar cómo entender los vasopresores, de una forma fácil y lógica. Para entender los vasopresores es crucial entender qué es el gasto cardiaco ("cardiac output" en inglés).
El gasto cardiaco es el volumen de sangre que el corazón bombea en un minuto. El cuerpo tiene aproximadamente de 5-6 litros de sangre. Para efectos de cálculo en esta discusión, escogeremos el valor de 5 litros (5,000 mL). Bajo circunstancias normales, los órganos importantes del cuerpo necesitan que el corazón pueda bombear esos 5 litros de sangre cada minuto. Cada uno de esos 5 litros de sangre está transportando oxígeno y glucosa a las células. El término perfusión precisamente describe el flujo de sangre a los tejidos del cuerpo. Si el gasto cardiaco disminuye, el flujo al cerebro y órganos importantes disminuye. Si el flujo disminuye, no hay suficiente perfusión a los órganos importantes.
¿Qué nos dice la presión sanguínea? Absolutamente NADA. Presión no es igual a flujo. Lo único que tiene relevancia clínica es que haya flujo hacia los órganos importantes. La presión sanguínea eventualmente va a caer, pero el hecho de que sea baja no implica necesariamente que no sea suficiente. Las guías de resucitación de trauma actualmente recomiendan que la presión se mantenga entre 80-90 mmHg. Una presión arterial en los 70s probablemente tendrá signos clínicos de pobre perfusión y de mecanismos de compensación inadecuados.
Por otro lado, una presión arterial relativamente normal puede ser el resultado del último esfuerzo desesperado y evidentemente fracasado de proteger a los órganos importantes. El confiar exclusivamente en la presión, y no mirar los demás factores asociados a la pobre perfusión podría ser peligroso.
Entonces, ¿debemos continuar usando la presión arterial como marcador principal? En mi atrevida opinión, NO.
La lectura de un electrocardiograma (ECG o EKG) de 12 derivaciones (12-lead, por su término en inglés) es una destreza básica de todo profesional de la salud envuelto en el manejo de un paciente críticamente enfermo.
- Frecuencia y ritmo
- Eje
- Intérvalos y Bloqueos
- Hipertrofias
- Electrolitos y drogas
- Imitadores de STEMI
- Isquemia e infarto
- Contexto